تقدم العلم في الآونة الأخيرة وقام الباحثون بأبحاث كثيرة لعلاج الأمراض المميتة كالسرطان، ونشروا الكثير من تلك الأبحاث في المجالات العلمية، ستجد في عدد ليس بقليل من تلك الأبحاث التي نُشِرَت أنهم استخدموا «الخلايا الجذعية (Stem Cells)».
فما هي الخلايا الجذعية؟ وما هو المختلف فيها؟ ما هي؟ أنواعها؟ وما هي استخداماتها؟
ما هي الخلايا الجذعية
إن جسم الإنسان يتكون من الكثير من الخلايا المتخصصة التي تقوم بوظائف محددة والتي تكون متمايزة، لكن الخلايا الجذعية هي نوع من الخلايا «اللامتمايزة Undifferentiated))» القادرة على التمايز إلى خلايا متخصصة (Specialized) بما فيها الخلايا الجذعية نفسها.
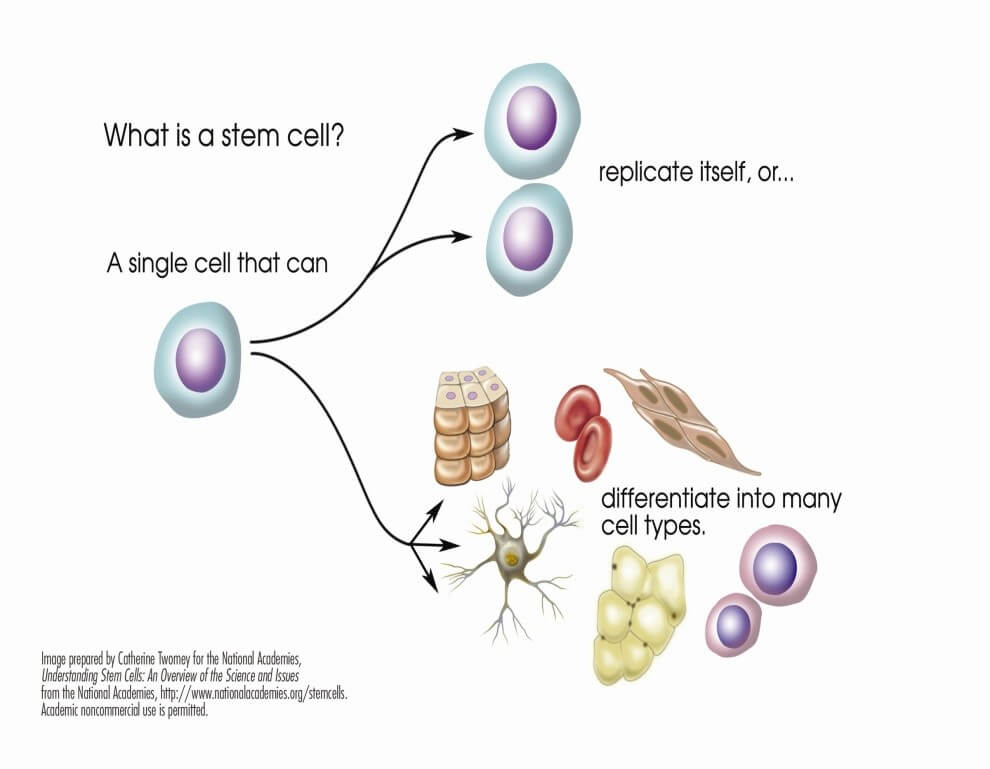
الخلايا الجذعية تعتبر لبنة الجسم الخام، وتقوم بدور مهم لجسم الإنسان من التطور الجنيني حتى البلوغ، تطور الخلية يبدأ عندما يندمج الحيوان المنوي بالبويضة لتنشأ البويضة المخصبة والتي تعتبر نوع خاص من الخلايا الجذعية التي لديها القدرة لتصبح إنسان كامل.
أنواع الخلايا الجذعية حسب مصدرها
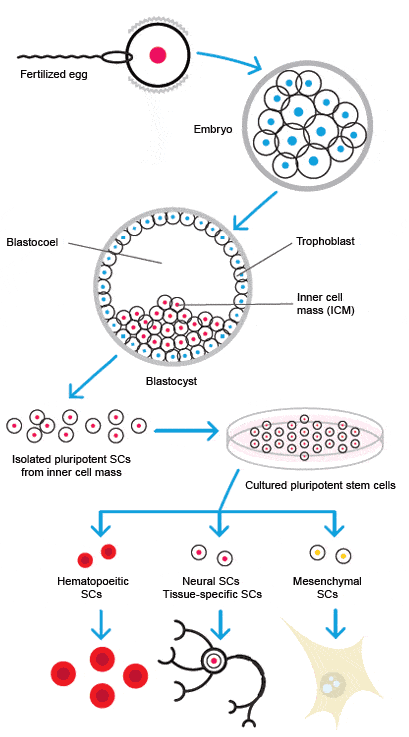
1- الخلايا الجذعية الجنينة ( Embryonic Stem Cells “ES” ):
يعتبر هذا النوع محور اهتمام العلماء أغلب تجاربهم العلمية كانت قائمة عليها، ولكن كانت تواجههم مشكلة أخلاقية ألا وهي أنهم لاستخراج تلك الخلايا وعزلها يجب عليهم أن يدمروا الجنين.
يتميز هذا النوع من الخلايا بميزتين رئيسيتين هما:
- تتواجد تلك الخلايا في كتلة الخلايا الداخلية (Inner Cell Mass) الموجودة في كيسة أريمية (Blastocyst).
- تتميز بأنها خلايا وافرة القدرات (Pluripotent) ، بمعنى أنها قادرة على تكوين ال 220 نوع من الخلايا التي يتكون منهم جسم الإنسان.
2- الخلايا الجذعية البالغة (Adult Stem Cells ):
الخلايا الجذعية البالغة لها دور مهم ورئيسي في نمو الخلايا وترميمها، أو استبدالها عندما تتلف.
يتميز هذا النوع من الخلايا بميزتين رئيسيتين هما:
- تتواجد تلك الخلايا في أنسجة الجسم مثل: نخاع العظم والأسنان وخلايا الجلد وغيرها من الأنسجة.
- تتميز بأنها عكس الخلايا الجذعية الجنينة فهي خلايا متعددة القدرات (Multipotent) ، بمعنى أنها قادرة على تكوين عدد محدود من الخلايا.
أهم ثلاثة خصائص التي تتميز بها الخلايا الجذعية بعيدًا عن مصدرها :
- لديها القدرة على الانقسام والتجدد لفترات طويلة وتسمى تلك العملية بالتكاثر (Proliferation)، بمعنى أنها قادرة على التجدد الذاتي (Self-renew).
- غير متخصصىة (Unspecialized) , وتلك أهم صفة تتميز بها الخلايا الجذعية بأنها ليس لها شكل ووظيفة محددة حتى تتخصص.
- لديها القدرة على أن تصبح خلايا متخصصة، وتسمى تلك العملية بالإختلاف الخلوي (Differentiation).
التفكير في طرق بديلة للحصول على الخلايا الجذعية
بسبب ندرة الخلايا الجذعية البالغة في الأنسجة وصعوبة الحصول على الخلايا الجذعية الجنينة وفصلها من غير قتل الجنين أصبح الشغل الشاغل للعلماء إيجاد حل لهذه المشكلة، وهو ما تم على يد العالم الياباني شينيا ياماناكا (Shinya Yamanka ).

الذي فاز على أثره بجائزة نوبل في الطب لعام 2012 ، ففي عام 2006 وجد يامانكا وفريقه حل لتلك المعضلة التي واجهت العلماء، ألا وهي الخلايا الجذعية المستحثة وافرة القدرات (Induced Pluripotent Stem Cells “IPS”) عن طريق إعادة البرمجة الجينية الخلوية (Genetic Cell Reprogramming ) ، هذا النوع من الخلايا مصنع معمليًا، و قد حل المعضلتين التي ذكرناهم سابقًا، وذلك عن طريق الإجابة على سؤال جوهري، وهو: هل يمكن عكس حالة التمايز الخلوي للخلية، وتحويلها لخلايا جذعية مرة أخرى ؟
فاتجه ياماناكا إلى مقارنة الخلايا الجسدية بالخلايا الجذعية على مستوى الجينات (Genes) ، لمعرفة الجينات المفعلة في الخلايا الجذعية الجنينة (Embryonic Stem Cells)، والتي تكسبها صفاتها فتوصل في النهاية إن جميع الخلايا الجذعية الجنينة تحتوي على 4 جينات رئيسية وهم:
- Oct-3/4
- c-Myc
- KLF4
- Sox2
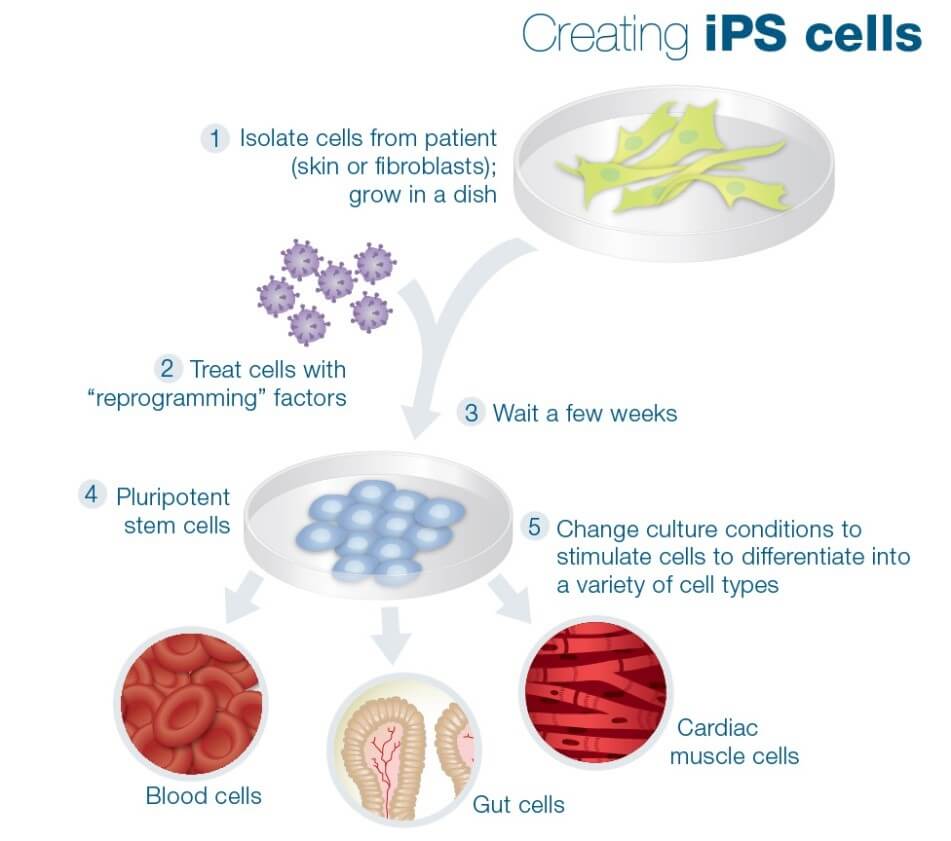
ولتصنيع تلك الخلايا الجذعية معمليًا قام ياماناكا بعمل الخطوات التالية:
1- فصل الأربع جينات الرئيسية وإدخالها إلى خلايا جلد، أو أرومة ليفية (Fibroblast) الذي يقوم بإنتاج النسيج الضام (Connective Tissue).
2- وضعها في مزرعة خلوية (Tissue Culture) عن طريق حوامل فيروسية من نوع (Retrovirus)، وتسمى تلك العملية بإعادة البرمجة (Cell Reprogramming).
3- يتركها لبضعة أسابيع لتتحول خلايا الجلد أو الأرومة الليفية إلى حالة تشبه الخلايا الجذعية الجنينة بحيث تكتسب قدرة (Pluripotent)، ولذلك سميت تلك الخلايا بالخلايا الجذعية المستحثة وافرة القدرات (Induced Pluripotent Stem Cells “IPS”)، وبذلك تم تحويل الخلايا المتمايزة إلى خلايا جذعية معمليًا مرة أخرى، و قد أحدث هذا قفزة علمية هائلة.
وعلى الرغم من أهمية الاكتشاف إلّا إنه ظل هناك مشكلتين هما:
- عدد قليل من الخلايا الجسدية يتم إعادة برمجته، حيث ينتج من كل 100 خلية جسدية يتم برمجتها خلية جذعية واحدة.
- استعمال الحوامل الفيروسية ووجود جين c-Myc يزيد من احتمال تحول الخلية إلى خلية سرطانية.
استخدامات الخلايا الجذعية:
ولكن على الرغم من تلك المشاكل، فإن هذا البحث قدم إضافة حقيقية في هذا المجال مما مهد لاستعمالها في الكثير من التطبيقات العلاجية، وإن من أهم الاستخدامات للخلايا الجذعية في الوقت الحالي تظهر في استزراع نخاع العظم Bone Marrow Transplant) ) في علاج مرض سرطان الدم (leukemia)، فنخاع العظم يحتوي على الخلايا الجذعية البالغة (Adult Stem Cells) القادرة على إنتاج جميع أنواع الخلايا التي يتكون منها دم الإنسان من كرات دم حمراء وكرات دم بيضاء بأنواعها والصفائح الدموية. وتستخدم تلك الطريقة في علاج الكثير من أمراض الدم ونخاع العظم وأيضا سرطان الدم والأمراض المناعية.
وفي الآونة الأخيرة بدأ استخدام الخلايا الجذعية في علاج الأمراض المرتبطة بالدم عن طريق الخلايا الجذعية من الدم المحيطي (Peripheral Blood Stem Cells “PBSCs”)، و تقنية تخزين الخلايا الجذعية من دم الحبل السري (Umbilical Cord Blood Ste Cells).
أحدث الطرق للحصول على الخلايا الجذعية وحفظها:
أحدث الاستخدامات وهي «الخلايا الجذعية من دم الحبل السري (Umbilical Cord Blood Stem Cells )» ، الأطفال حديثو الولادة لا يحتاجون الحبل السري فبالعادة كان يتم التخلص منه بعد الولادة ، ولكن هذا تغير في الأعوام القليلة الماضية، فقد وجدوا أن العلاج عن طريق خلايا الدم الجذعية الموجودة في الحبل السري أثبتت جودته في علاج الأمراض مقارنة بطريقة العلاج بالخلايا الجذعية الموجودة في نخاع العظم, أو في الدم المحيطي ، وذلك لسببين مهمين، وهما:
1- السبب الأول: أن استزراع خلايا الدم الجذعية الموجودة في الحبل السري أقل قابلية للرفض من الجسم مقارنة بالطريقتين ؛ لأن تلك الخلايا لم يكتمل نموها و خصائصها بالشكل الكافي ليتم التعرف والهجوم عليها من المستقبلات في الجهاز المناعي (Immune System) للجسم .
2- السبب الثاني: أن خلايا المناعية للدم في الحبل السري لم تتطور بالشكل الكافي القادر على مهاجمة جسم المتلقي لعملية الاستزراع والتي تسمى بداء الطعم حيال الثوي
(Graft Versus Host Disease “GVHD” ) بلفظ آخر رفض الأعضاء المزروعة
(Transplant Rejection) هو أحد أكثر المضاعفات تعقيدًا، التي تظهر بعد إجراء عملية زرع لعضو، أو خلية جذعية، أو نخاع العظم.
ما يحدث هو ردة فعل مناعية حادة جدًا يهاجم على أثرها جهاز المناعة العضو أو النسيج المزروع. في مثل هذه الحالات يعتبر جهاز المناعة العضو المزروع جسمًا غريبًا، ويقوم بإنتاج أجسام مضادة (Antibody) تلحق الضرر بجودة العضو المزروع و باحتمالات نجاحه.
وتعتمد تلك التقنية على أخذ الدم الموجود في الحبل السري للجنين بعد الولادة مباشرة تحديداً في المرحلة الثالثة من الولادة قبل المشيمة حيث يقوم طاقم طبي بسحب الدم من وريد الحبل السري بعد تعقيمه، وتستغرق عملية الجمع من 2 إلى 4 دقائق فقط وتخزينه في حاوية في بنك عن طريق التبريد في درجة حرارة من -200 درجة بواسطة النيتروجين السائل، وتبقى هذه الوحدة جاهزة للاستعمال من 15 إلى 20 سنة، بحيث يتم استعمال الخلايا الجذعية التي فيه في المستقبل للأبحاث أو العلاج.
بنوك الخلايا الجذعية في العالم والشرق الأوسط
بالنسبة للعلاج، فبنوك خلايا دم الحبل السري تكون خاصة، وفيها يتم تخزين الخلايا الجذعية من دم الحبل السري للشخص عند ولادته وتحفظ باسمه، وتكون هذه الخلايا في متناوله حيث يمكنه الحصول عليها مستقبلا عند الحاجة مثل مرض أحد أفراد الأسرة وهكذا.
وهذه الخدمة تقدم نظير مبلغ محدد يتضمن مصاريف جمع العينة وتخزينها على مدار السنوات القادمة، وهناك في العالم العربي أكثر من بنك منهم بنك الخلايا الجذعية ف مصر CellSafe Cord Blood Bank الذي تأسس عام 2009، وهو معتمد من وزارة الصحة المصرية ومن هيئة الرابطة الأمريكية لبنوك الدم AABB، وهناك أول بنك للخلايا الجذعية من دم الحبل السري في الشرق الأوسط CryoSave The Family Stem Cell Bank وله فروع في الإمارات العربية المتحدة وجمهورية مصر العربية والسعودية وبعض الدول العربية الأخرى.
______________
إعداد:Ahmed Nouh
تدقيق: Bara’a Thweib
تصميم: Omar Khaled
المصادر:
- https://goo.gl/BXiJk8
- https://goo.gl/N1jzeb
- https://goo.gl/itrQ68
- https://goo.gl/ZNTpy1
- https://goo.gl/KVpVDp
- https://goo.gl/4CyXgb